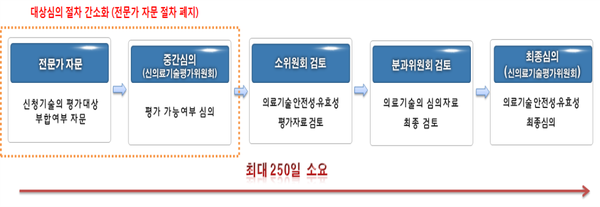
 ▲ 절차 간소화를 통해 신의료기술 평가기간이 단축된다.
▲ 절차 간소화를 통해 신의료기술 평가기간이 단축된다.3D프린팅, 인공지능(AI), 로봇 등 신의료기술 평가기간이 단축되고 별도의 평가트랙이 도입됨에 따라 시장 조기진입 활성화가 기대되고 있다.
보건복지부(장관 박능후)는 이같은 내용을 담은 ‘신의료기술평가에 관한 규칙’ 개정안을 3월 15일 공포·시행한다고 밝혔다.
이번 개정안은 지난해 7월 정부가 발표한 ‘의료기기 규제혁신 및 산업육성방안’의 일환으로 인공지능(AI), 3D 프린팅, 로봇 등 첨단기술이 융합된 혁신의료기술에 대한 신의료기술 평가기간 단축과 혁신의료기술 별도평가트랙 도입이 주요 내용이다.
이에 따라 신의료기술 평가시 전문가 서면 자문을 통해 신의료기술평가 대상 여부를 판단했던 절차가 내부 평가위원으로 대체해 2단계의 평가절차를 1단계 평가절차로 줄어든다. 외부 전문가 탐색 및 구성 등으로 인해 발생했던 시간을 절약됨에 따라 신의료기술평가의 기간은 기존 최대 280일에서 250일로 30일 가량 줄어든다.
암, 심장질환 등 중증 질환을 치료하거나 환자의 만족도를 증진시키는 의료기술에는 기존의 신의료기술평가가 아닌 별도의 평가트랙이 적용된다. 이번에 도입된 ‘혁신의료기술 별도평가트랙’에서는 기존의 문헌 평가와 더불어 새로 개발된 의료기술의 잠재성 평가까지 진행한다.
이에 따라 기존의 평가체계에서 유효성을 평가할 문헌이 부족하여 탈락했던 의료기술 중 환자의 삶을 획기적으로 개선하거나 환자의 비용 부담을 줄여주는 등 높은 잠재성을 가졌을 경우, 조기 시장 진입이 허용된다. 다만, 혁신의료기술이라 하더라도 사람의 인체 조직 내부에 행해지는 환자의 부담이 큰 의료기술에 대해서는 문헌을 통한 엄격한 안전성 검증이 실시된다.
또한 ‘혁신의료기술 별도평가트랙’을 통해 의료현장에 도입된 혁신의료기술은 의료현장에서 활용된 결과를 바탕으로 3~5년 후 재평가를 받아야 한다. 이를 위해 이를 위해, 혁신의료기술을 개발한 의료기기 업체 등은 수집되는 자료 등을 한국보건의료연구원에 제출해야 하며 이를 어길 경우 혁신의료기술의 사용이 중단될 수 있다.
보건복지부 손호준 의료자원정책과장은 “신의료기술 평가기간을 단축시킴으로서, 다소 긴 평가기간으로 인해 어려움을 호소했던 의료기기 업체들의 부담도 줄어들 것”이라며 “혁신의료기술 별도평가트랙의 도입을 통해 그간 늦어졌던 혁신의료기술의 활용을 촉진하되, 의료기술의 안전성은 엄격히 검증할 예정”이라고 밝혔다.
